Las deficiencias micronutricionales crónicas pueden conducir a desórdenes metabólicos que, con el paso de los años, sientan las bases de patologías severas. El sistema inmunitario se debilita, incrementando la prevalencia de enfermedades infecciosas y susceptibilidad a patologías degenerativas crónicas, así como una afectación directa sobre el desarrollo mental, físico y capacidad funcional en general.
Los fármacos y micronutrientes comparten el mismo transporte y las vías metabólicas en el organismo para su absorción intestinal, metabolismo y excreción. De esta manera, cuando se administran uno o más fármacos siempre existe un riesgo potencial de interacción con el estado micronutricional del paciente.
Inhibidores de la bomba de protones (IBP)
Los inhibidores de la bomba de protones (IBP) bloquean la ATPasa H+/K+ gástrica inhibiendo la secreción de ácido gástrico. El incremento del pH intragástrico por los IBP altera la absorción y utilización de micronutrientes como el hierro, calcio, magnesio, vitamina C y vitamina B12.
IBP y vitamina B12
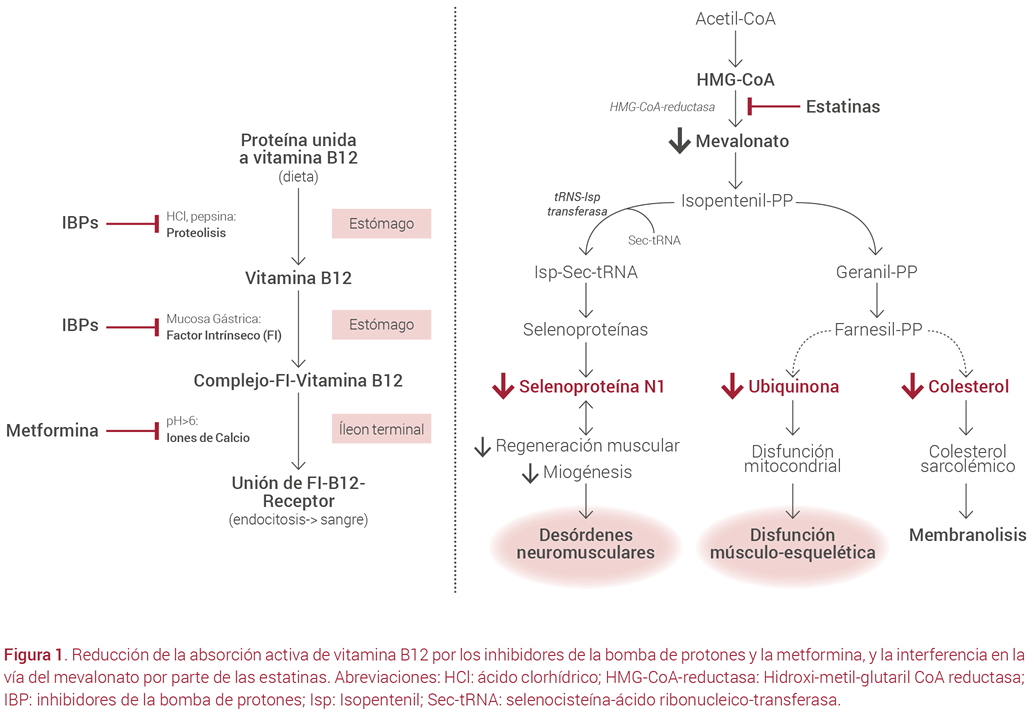
El incremento del pH intragástrico por los IBP, por un lado, altera la absorción activa de la vitamina B12, limitando la separación de vitaminas de las proteínas de la dieta (Figura 1), y por el otro, conduce a la alcalinización del medio del intestino delgado, eliminando la barrera fisiológica a microorganismos, de manera que bacterias de la parte baja del intestino pueden incrementar y entrar en el yeyuno y el íleon. El sobrecrecimiento bacteriano con Clostridios y Campylobacter se acompaña por un incremento en el consumo de B12 y síntesis bacteriana de sustancias que compiten por los receptores en la mucosa del íleon.
La influencia de los IBP en la malabsorción de la vitamina B12 es claramente dosis-dependiente. Un estudio de cohortes prospectivo con pacientes infectados por Helicobacter pylori mostró que el 33% de los pacientes tratados con omeprazol durante 5 años desarrollaron gastritis atrófica con un descenso significativo de los niveles séricos de vitamina B12. Además, pacientes con un polimorfismo genético del citocromo P450, CYP2C19, que cataliza el metabolismo del omeprazol, sufren el riesgo de reducciones en los niveles séricos de vitamina B12 en pacientes bajo tratamientos a largo plazo. Finalmente, en un estudio en el que se comparó una población diagnosticada con deficiencia en vitamina B12 con un grupo sin diagnóstico de déficit, se concluyó que la utilización previa de IBP durante 1 o 2 años, se asoció con un incremento en el riesgo de deficiencia de B12 en un 65%.
IBP y hierro (Fe)
El estado físico del Fe que entra en el duodeno tiene mucho que ver en su absorción. A un pH fisiológico, el ion ferroso (Fe2+) se oxida rápidamente a la forma férrica (Fe3+) que es insoluble. El ácido gástrico desciende el pH en el duodeno proximal reduciendo el Fe3+, permitiendo el transporte del Fe2+ a través de la membrana apical de los enterocitos. Es esperable entonces, que si la producción de ácido gástrico se altera por la acción de los IBP, la absorción del Fe se reduzca de forma sustancial.
Un estudio de cohortes retrospectivo mostró que la utilización a largo plazo de IBP provoca un descenso de la mayoría de valores hematológicos, incluyendo la hemoglobina, hematocrito y el volumen corpuscular medio, comparado con el grupo control.
| Fármaco | Micronutriente | Efecto Adverso | Factores de riesgo añadidos |
| IBP | Vitamina B12 | ↓Absorción | Infecciones por Helicobacter pylori, gastritis atrófica, hipoclorhidria, edad > 60 años, metformina |
| Hierro | ↓Absorción | Cualquier causa de hipoclorhidria, vegetarianismo, edad > 60 años, deficiencia de Fe | |
| Magnesio | ↓Absorción | Diabetes, hipomagnesemia, diuréticos, edad > 60 años | |
| Diuréticos | Magnesio | ↓ Excreción renal | Hipertensión, diabetes, insuficiencia renal, actividad deportiva intensa, edad > 60 años |
| Estatinas | Vitamina D | Hipovitaminosis D incrementa el riesgo de SAMS | Edad > 60 años, patología cardiaca, osteoporosis, diabetes |
| Coenzima Q10 | ↓ Biosíntesis endógena | Diabetes, patología cardiaca, edad > 60 años, antidepresivos, actividad deportiva intensa | |
| Selenio | ↓ Síntesis de Selenoproteínas | Diabetes, patología cariaca, patología tiroidea, edad > 60 años | |
| Metformina | Vitamina B12 | ↓ Absorción | Vegetarianismo, edad > 60 años, demencia, deficiencia de folato, disfunción cognitiva |
IBP y magnesio (Mg)
La absorción y excreción de Mg está influenciada por diferentes hormonas. Se ha demostrado que la 1,25-dihidroxivitamina D puede estimular la absorción intestinal de Mg. Por otra parte, el Mg es un cofactor necesario para la unión de la vitamina D a su receptor VDR (Vitamin D Receptor). Además, la conversión de la vitamina D en su forma activa a través de las hidroxilaciones hepática y renal, es Mg dependiente. Cuando los niveles de Mg descienden, se altera la secreción de PTH inducida por bajos niveles de calcio.
La utilización a largo plazo de IBP se ha asociado en algunos casos a hipomagnesemia, hipocalcemia e hiperparatiroidismo. La monitorización de los niveles de Mg, especialmente en aquellos con diabetes y patología cardiovascular y utilización a largo plazo de los IBP, es especialmente importante, ya que la probabilidad y el riesgo de complicaciones asociadas a su patología es elevada.
Los IBP descienden la absorción intestinal de Mg, interfiriendo tanto en la absorción pasiva como activa. Igualmente, se ha identificado un polimorfismo en el gen TRPM6, que puede incrementar el riesgo de hipomagnesemia en pacientes tratados con IBP.
Publicaciones recientes, basadas en estudios de cortes transversales y estudios clínicos, indican que alrededor del 10-30% de la población considerada saludable, tiene una deficiencia subclínica de Mg. En mujeres postmenopáusicas con osteoporosis asciende al 84%, en postoperatorios de pacientes críticos es del 36.5% y en los mayores, especialmente en mujeres, llega al 30%.
Diuréticos tiazídicos (TDZ)
Es el segundo fármaco antihipertensivo más recetado y aunque son los diuréticos mejor tolerados entre los fármacos antihipertensivos, suelen asociarse a alteraciones electrolíticas, ácido-base y metabólicas. Dependiendo de modo de acción, algunos diuréticos incrementan la excreción de potasio, magnesio, cloruro, calcio o bicarbonato.
TDZ y Magnesio (Mg)
En general los TDZ se asocian a un descenso de los niveles de Mg sérico de un 5-10%, es más, hasta el 50% de los pacientes tratados presentan una depleción de Mg a nivel celular, independientemente de las concentraciones séricas normales.
Es importante destacar que el Mg es un segundo mensajero para la acción de la insulina, concretamente en la actividad de la tirosina quinasa del receptor de la insulina y en la actividad de la proteína transportadora de glucosa, GLUT4, ayudando a regular la translocación de la glucosa al interior de la célula. Por lo tanto, un déficit intracelular de Mg puede afectar al riesgo de la resistencia a la insulina y alterar la entrada de glucosa a la célula. Es lógico entonces que la deficiencia subclínica de Mg y su depleción intracelular asociada al tratamiento con TDZ puedan interferir con la actividad de la tirosina quinasa y en el receptor de la insulina, incrementando el riesgo de resistencia a la insulina.
En un estudio reciente la constante suplementación oral con Mg en pacientes hipertensas tratadas con TDZ se asoció a una mejora en el control de la presión sanguínea, la función endotelial y la aterosclerosis subclínica.
Las estatinas
Las estatinas reducen la síntesis de colesterol en el hígado inhibiendo de forma competitiva la enzima HMG-CoA reductasa. Pueden causar diversos efectos secundarios, incluyendo molestias músculo esqueléticas (miositis), fatiga, incomodidad gastrointestinal, elevación de enzimas hepáticas, síntomas neurocognitivos, neuropatías periféricas e insomnio. Los síntomas musculares asociados a las estatinas (SAMS, Statin Associated Muscle Symptoms) se presentan del 10 al 29% de los pacientes y es de los efectos secundarios más prevalentes. La insuficiencia en vitamina D, la depleción de Q10 inducida por las estatinas y/o el efecto negativo de las estatinas en la síntesis de selenoproteínas, se han relacionado con la patogenia de los síntomas miopáticos.
Estatinas y Vitamina D
La forma hormonalmente activa de la vitamina D, 1α,25-dihidroxivitamina D no es únicamente un regulador de la homeostasis del calcio y el fosfato, sino que su receptor VDR, ha sido detectado en más de 35 tejidos que no están involucrados en el metabolismo óseo. Entre ellos se incluyen las células endoteliales, células de los islotes del páncreas, células hematopoyéticas, células cardíacas y músculo-esqueléticas, monocitos, neuronas, células placentarias y los linfocitos T.
Diversos estudios han demostrado el papel potencial de la vitamina D para la prevención y tratamiento de los SAMS. La prevalencia de mialgias en pacientes tratados con estatinas e insuficiencia de vitamina D es significativamente elevada comparada con los que no presentan signos de SAMS. Además, los resultados de un estudio de cohorte retrospectivo y un metaanálisis de 7 estudios con 2420 pacientes ha evidenciado que bajos niveles de vitamina D se asocian con mialgias en pacientes tratados con estatinas.
Estatinas y coenzima Q10 (CoQ10)
La vía del mevalonato es uno de los procesos metabólicos más importantes dentro de la célula regulado por la HMG-CoA reductasa (Figura 1). Las estatinas inhiben la HMG-CoA reductasa, inhibiendo la producción de mevalonato, un precursor tanto del colesterol como de la ubiquinona.
La depleción de ubiquinona inducida por las estatinas atenúa la transferencia de electrones en la cadena de transporte de electrones con efectos deletéreos en la función muscular. Algunos estudios en pacientes con SAMS, también demuestran un descenso significativo en los niveles musculares de CoQ10. Por otro lado, en un estudio randomizado pacientes con SAMS recibieron diariamente o CoQ10 o vitamina E durante 30 días. Después de 30 días de suplementación con CoQ10 la severidad del dolor descendió significativamente hasta el 40% y la interferencia del dolor con las actividades diarias se redujo hasta un 38%. En otro estudio randomizado la suplementación con CoQ10 durante 30 días redujo el dolor muscular en el 75% de los pacientes.
Estatinas y selenio (Se)
Los efectos secundarios musculares asociados con el tratamiento de estatinas son muy similares a los síntomas de la deficiencia de Se. Las estatinas pueden interferir con la ruta bioquímica de la isopentenilación del ARN-t de la selenocisteína (Figura 1). Los efectos negativos de las estatinas en la síntesis de selenoproteínas parece explicar algunos de los efectos musculares de las estatinas, concretamente la miopatía. La selenoproteína N (SEPN) se expresa de forma ubicua y es esencial para la regeneración muscular. La deficiencia de selenoproteína N causa diversas alteraciones neuromusculares y reciben el nombre de miopatías SEPN.
Metformina
Metformina y vitamina B12
La prevalencia de deficiencia de vitamina B12 en pacientes con metformina es aproximadamente del 9.5 al 20% y los ensayos aleatorizados nos indican que los niveles séricos de vitamina B12 están inversamente asociados con la dosis y la duración del uso de la metformina.
La Figura 1 muestra el mecanismo de acción por el cual la metformina desciende los niveles de vitamina B12.
Diversos estudios han demostrado una posible relación causal entre la depleción de vitamina B12 inducida por la metformina con la disfunción cognitiva, neuropatía periférica, alteraciones hematológicas y niveles elevados de homocisteína.
Además, la metformina no sólo induce la depleción de vitamina B12, sino que de forma progresiva incrementa el ácido metilmalónico (MMA), un biomarcador funcional de alta sensibilidad para la deficiencia de vitamina B12.
Por lo tanto, en pacientes con diabetes tipo 2 tratados con metformina, especialmente aquellos con el uso concomitante de IBP, es recomendable monitorizar los niveles de vitamina B12 y/o los de homocisteína.
Debido al incremento continuo de fármacos y de la frecuencia con la que se usan, es imprescindible prestar atención particular a los efectos adversos de los fármacos en los niveles micronutricionales, para minimizar el riesgo potencial para la salud de los pacientes (Tabla 1). Especialmente en aquéllos con un alto riesgo (edad avanzada, polimedicados) y personas bajo medicación con fármacos como los inhibidores de la bomba de protones, diuréticos y/o estatinas.
Uwe Gröber, Joachim Schmidt, Klaus Kisters. Important drug-micronutrient interactions: a selection for clinical practice. Critical Reviews in Food Science and Nutrition. 2020 Vol. 60, 2, 257-275.

CN Base aporta equipos micronutricionales de vitaminas, minerales y dosis efectivas de factores vitamínicos como coenzima Q10 y ácido R-lipoico. Estos conjuntos micronutricionales se presentan en las formas moleculares clave para poder ser absorbidas en caso de ser portadores de polimorfismos genéticos poco favorables. Se aportan las vitaminas en forma activa (L-metilfolato, metilcobalamina, dibencozida, riboflavina 5’fosfato y piridoxal 5’fosfato), que junto con los otros coenzimas vitamínicos y cofactores metálicos, ayudan a recuperar el estado micronutricional óptimo en los casos en los que existe la administración de fármacos a largo plazo.
CN Base forma parte del programa de La Micronutrición Básica.
La Micronutrición Básica se compone de CN Base o Petit CN Base, Omega Base y Amino Base, que aporta los conjuntos micronutricionales necesarios para un óptimo funcionamiento del organismo. En su composición se escogen los micronutrientes más biodisponibles, bioidénticos y/o bioaccesibles por el organismo, para facilitar la mayor impregnación de los micronutrientes en tejidos y células. No interaccionan con los fármacos y pueden ser administrados a cualquier persona independientemente de la edad, sexo o condición de salud.
Petit CN Base es un conjunto equilibrado de los 23 micronutrientes más importantes para un óptimo desarrollo, junto a FOS y S.boulardii. Es un complemento micronutricional para el embarazo, lactancia y niños en crecimiento, compuesto por vitaminas, minerales, colina, fructooligosacáridos de cadena corta con acción prebiótica y Saccharomyces boulardi con acción probiótica. Entre las vitaminas destacan las formas activas más biodisponibles de ácido fólico (metilfolato), vitamina B12 (metilcobalamina); vitamina B6 (piridoxal 5-fosfato); vitamina B2 (riboflavina 5-fosfato); vitamina D (colecalciferol), vitamina A (retinol)… Entre los minerales, encontramos el hierro aminoquelado, el zinc en forma de gluconato junto con otros minerales en forma de citratos
Omega Base es un complemento micronutricional a base de ácidos grasos omega 3 y omega 6. Aporta un alto y equilibrado contenido en ácidos grasos poliinsaturados omega 3 y omega 6, en una combinación y proporción que consiguen la mayor actividad biológica, impregnando la membrana plasmática y asegurando la formación de fosfolípidos y eicosanoides adecuados para el control de la inflamación crónica de bajo grado.
Amino Base es el conjunto equilibrado de aminoácidos esenciales y condicionalmente esenciales en forma libre, junto con nucleótidos, citidina, uridina y factores vitamínicos como colina y mioinositol.